副反应产物氧化亚铜在化学镀铜溶液中的危害很大,因为氧化亚铜会进一步发生还原反应和歧化反应
生成的铜单质弥散在溶液中成为催化活性中心,使镀液崩溃或附着在工件上成为铜粉使工件变得粗糙。抑制产生氧化亚铜和铜粉的方法有三种。一是在溶液中通入空气使Cu2O重新氧化为Cu2+
本文使用PEG6000作为乙二胺四乙酸(EDTA)/四羟丙基乙二胺(THPED)二元络合化学镀铜体系的表面活性剂,系统研究PEG6000对化学沉积铜混合电位、沉积速率和镀层形貌与晶体结构的影响。
1 实验方法
1.1 实验用试剂
实验用试剂有:CuSO4、EDTA和甲醛为上海凌峰化学试剂;PEG6000和NaOH为国药试剂;2,2’-联吡啶为阿拉丁试剂;四羟丙基乙二胺(THPED)为陶氏化学试剂。
1.2 化学镀铜样品的制备
采用纯铜片(150 mm×100 mm×0.5 mm)作为化学镀的基体材料,铜片化学镀的前处理为:无水乙醇清洗→水洗→5%NaOH除油→去离子水清洗→微蚀溶液(5%柠檬酸+5%过硫酸钠)浸渍5~10 s→蒸馏水冲洗→40 mg/L的PdCl2溶液活化2~5 min→蒸馏水冲洗→干燥称重,经前处理好的铜片放入化学镀铜溶液中镀覆,温度采取水浴控制,维持在50℃,化学镀60 min后取出试片干燥称重,再进行表面结构表征。化学镀铜的基础配方如表1:
表1 化学镀铜溶液的组成
Table1
| PEG 6000/mg·L-1 | Other items |
|---|---|
| 20 | CuSO4∙5H2O: 0.05 mol/L |
| 25 | EDTA: 0.03 mol/L |
| 30 | THPED: 0.025 mol/L |
| 35 | NaOH: 0.2 mol/L |
| 40 | Formalin: 0.1 mol/L 2,2’-dipyridyl: 8 mol/L |
1.3 镀速的测定
用增重法计算沉积速率:
式中v为沉积速率,即镀速(μm·h);Δm为施镀前后的质量差(g);t为化学镀时间(h);S为试片镀覆面积(cm2);ρ为铜的比重(8.9 g·cm-3)。
1.4 化学镀液的电化学测试
使用CHI660E电化学分析仪,采用传统三电极体系测试不含PEG和含PEG表面活性剂对比的镀液混合电位和线性扫描曲线。Ag/AgCl为参比电极,Pt为辅助电极,工作电极为环氧树脂冷镶嵌的纯Cu圆电极(面积为1 cm2)。测试前依次用800#、1200#和2000#金相砂纸抛磨,再用氧化铝抛光膏抛光至镜面。线性扫描测试伏安阴极还原曲线时,溶液中不含还原剂甲醛。阳极氧化测试时,溶液中不含硫酸铜。扫描电势范围均从-0.20 V到-0.60 V,扫描速率均为2 mV/s。混合电位的测试溶液按表1中给出的条件进行,时间为400 s,扫描速度为0.1 s记录一次数据,其开路电位(OCP)即体系的混合电位。
1.5 镀层结构的分析
用JSM-6480LV型扫描电子显微镜观察化学镀铜层表面形貌和元素组成;用RigaKu Ultima Iv型X射线衍射仪(Cu靶,Κα=0.15418 nm,管电压40 kV,管电流40 mA,扫描速度为10°/min)测定化学镀铜层的晶体结构。
2 结果和讨论
2.1 PEG6000浓度对体系混合电位的影响
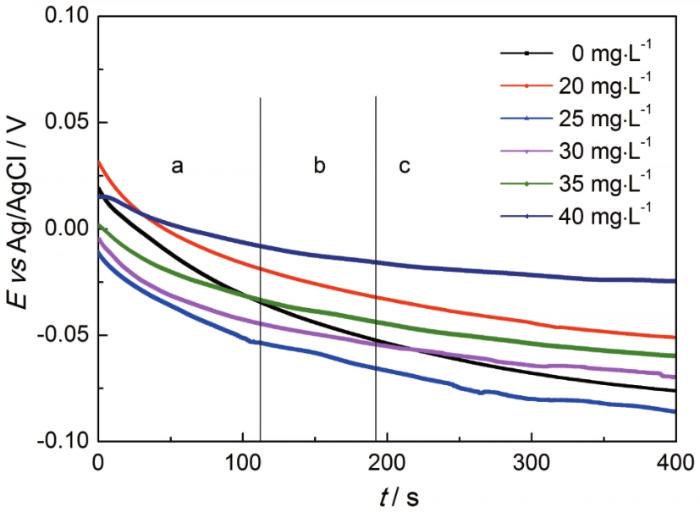
图1给出了含有不同浓度PEG6000的化学铜镀液在纯铜电极表面的混合电位-时间(Emix-t)曲线。由图1可见,铜电极在化学铜镀液中的混合电位-时间(Emix-t)曲线分为三个区:诱发区(Induction region,图中a区)、过渡区(Transitional region,图中b区)和稳定区(Stable region,图中c区)[30]。在初始约110 s的诱发区内混合电位下降较快,因为电极与化学镀液的固液两相接触后负电性离子(如OH-)的半径比正电性离子(如[CuL]2+)的半径小得多,故扩散迁移速度较快。因此,大量负电性粒子和少量正电性粒子吸附到电极表面,使电极表面的电位很快负移;随着离子的积累氧化还原反应在其表面进行,正电性铜络合离子和负电性OH-逐级被消耗,而正电性铜络合离子迁移速度仍慢于OH-的迁移。因此,负电性离子补充快于正电性离子,使电位继续负移,但是负移速度比诱发区即过渡区的低;达到一定时间(约180 s)后,电位、反应气泡的强化扩散、浓度差等因素使正负离子的消耗与补充逐渐趋于平衡,混合电位也趋于稳定,此时即稳定区,三个区域没有明显的分界。
图1
图1
PEG6000浓度不同时铜电极表面的混合电位-时间曲线
Fig.1
Emix-t curves under different PEG6000 concentration
加入PEG6000添加剂使化学镀液的混合电位负移数值ΔU减小,如表2所示。ΔU值从0 mg/L的0.095 V减小到40 mg/L的0.043 V。PEG6000吸附在铜电极表面,阻滞了带电粒子在电极上的吸附,减少了电极活性面积,使负电性离子的相对电荷密度下降,使ΔU值减少。PEG6000浓度越高使吸附比越高,电位的负移值ΔU越小。
表2 不同PEG6000浓度的混合电位负移值
Table 2
| PEG6000/mg·L-1 | 0 | 20 | 25 | 30 | 35 | 40 |
|---|---|---|---|---|---|---|
| Fall-off value of EmixΔU/V | 0.095 | 0.082 | 0.071 | 0.064 | 0.059 | 0.043 |
2.2 不同PEG6000浓度时线性扫描曲线
图2
图2
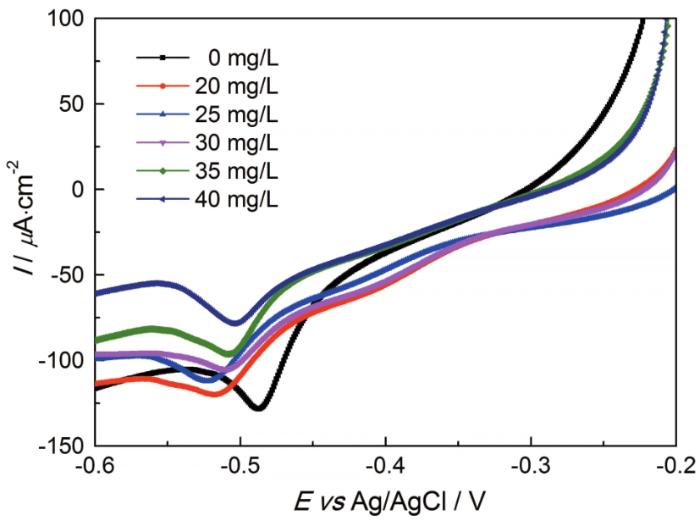
PEG6000浓度对Cu(II)离子阴极还原的影响
Fig.2
Influence of PEG6000 concentration on the cathodic reduction of Cu(II)ion
表3 不同PEG6000添加剂浓度的阴极还原峰值
Table 3
| Concentration of PEG6000/mg·L-1 | 0 | 20 | 25 | 30 | 35 | 40 |
|---|---|---|---|---|---|---|
| Reduction current density/µA·cm-2 | 131 | 120 | 112 | 105 | 96 | 78 |
图3
图3
PEG6000浓度对甲醛阳极氧化的影响
Fig.3
Influence of PEG6000 concentration on the anodic oxidation of formaldehyde
表4 PEG6000浓度不同的阳极氧化峰电流密度值
Table 4
| Concentration PEG6000/mg·L-1 | 0 | 20 | 25 | 30 | 35 | 40 |
|---|---|---|---|---|---|---|
| Oxidation current density/µA·cm-2 | 471 | 567 | 622 | 751 | 871 | 975 |
2.3 PEG6000对镀速的影响
图4给出了不同PEG6000浓度条件下化学镀铜的沉积速率。可以看出,随着PEG6000浓度的提高沉积速率相应降低,镀速由0 mg/L的7.51 μm/h下降到40 mg/L的4.08 μm/h。这与前文混合电位变化及线性扫描结果相一致,即PEG6000因吸附使二元络合体系混合电位的负移减缓,降低了反应驱动力,使阴极反应电流密度即铜沉积速率下降。对沉积速率曲线的拟合结果表明,镀速(V)与PEG6000浓度呈线性递减关系,可表示为
式中,C为PEG6000浓度(mg/L)。
图4
图4
PEG6000浓度对沉积速率的影响
Fig.4
Effect of PEG6000 concentration on the copper deposition rate
2.4 PEG6000对化学沉积铜表面形貌和结构的影响
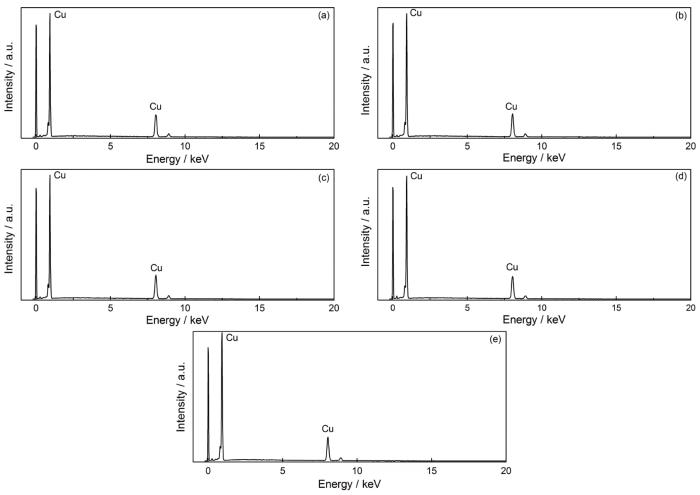
图5和图6分别给出了不同PEG6000浓度时化学沉积铜的SEM和EDS表征结果。可以看出,所制备的镀层表面平滑致密,没有铜粉铜瘤。PEG6000浓度不同时沉积的镀层表面宏观形貌没有明显的不同,即对沉积结晶的影响不大。图6给出了沉积铜的EDS分析,可见只有铜的特征峰。图7给出了沉积铜的XRD衍射图,在2θ为43.0±0.2°、50.1±0.2°和73.9±0.2°分别出现(111)、(200)和(220)衍射峰,与粉末衍射标准(PDF卡片编号040836)[31]的面心立方点阵结构(43.297°;50.433°;74.140°)十分接近,并且没有出现Cu2O等杂质峰,表明化学沉积铜纯度很高。根据表5给出的各晶面衍射峰强度占比分析,随着PEG6000浓度的提高(111)和(200)晶面占比均下降,而(220)比例增大,占比从37.3%升至49.0%。这表明,PEG6000使铜镀层向(220)晶面择优取向转变。
图5
图5
不同PEG6000浓度的化学沉积铜的SEM照片
Fig.5
SEM micrographs at different PEG6000 concentration (a) 20 mg, (b) 25 mg, (c) 30 mg, (d) 35 mg, (e) 40 mg
图6
图6
不同PEG6000浓度的化学沉积铜的EDS图
Fig.6
EDS micrographs at different PEG6000 concentration (a) 20 mg, (b) 25 mg, (c) 30 mg, (d) 35 mg, (e) 40 mg
图7
图7
不同PEG6000浓度化学镀铜沉积层的XRD谱图
Fig.7
XRD patterns of electroless copper layer at different PEG6000
表5 不同PEG6000浓度下铜镀层晶粒尺寸和特征衍射峰强度比
Table 5
| Concentration of PEG6000/mg·L-1 | Crystallite size/nm | I(111)/% | I(200)/% | I(220)/% |
|---|---|---|---|---|
| 20 | 77.7 | 36.7 | 25.9 | 37.3 |
| 25 | 69.3 | 34.0 | 26.4 | 39.6 |
| 30 | 59.5 | 32.6 | 24.0 | 43.4 |
| 35 | 52.2 | 31.5 | 23.2 | 45.3 |
| 40 | 50.0 | 27.1 | 23.9 | 49.0 |
根据各晶面衍射峰的半高宽,使用Scherrer公式[32,33]
可计算化学沉积的铜层平均晶粒尺寸。式中Κ为Scherrer常数,通常取值为0.89,λ为X射线的波长(0.15418 nm),β为衍射峰的半高峰宽(FWHM),θ为布拉格衍射角。
3 结论
(1) PEG6000使乙二胺四乙酸(EDTA)/四羟丙基乙二胺(THPED)二元络合体系化学镀铜的混合电位负移的趋势趋缓,因为PEG6000作为表面活性剂在铜表面的吸附减少了活性面积,阻滞了带电离子在电极表面的吸附,使负电性离子的相对电荷密度降低。
(2) PEG6000的吸附作用减缓了阴极还原反应,促进了阳极氧化反应,但是因为阴极还原反应为控制步骤,PEG6000降低了化学镀铜沉积速率,且铜的沉积速率随着PEG6000浓度的提高呈线性递减趋势。
(3) 在EDTA/THPED二元体系中制备的化学镀铜纯度较高,镀层表面平滑致密,没有铜粉或铜瘤;随着PEG6000浓度的提高镀层呈现(220)晶面择优取向的趋势;铜晶粒的尺寸由77.7 nm减小到50.0 nm,表明PEG6000能细化晶粒。