1 实验方法
1.1 材料的制备
将体积比为3∶2的无水乙醇和钛酸丁酯加入烧杯中,配制成溶液A;将去离子水、冰乙醇、无水乙醇以4∶4∶15的体积比混合,配制成溶液B;将溶液B滴加入溶液A中持续搅拌,将生成的溶胶在烘箱中烘干。将烘干后的溶胶在650℃保温1 h,得到纯TiO2粉体。
在溶液B中加入适量的硫酸铜后按上述步骤进行,制得Cu/Ti的原子比分别为1%、2%、3%的Cu掺杂TiO2。
1.2 性能表征
用DX-2700型X射线衍射仪(XRD)表征样品晶体结构;用Hitachi SU8220型扫描电子显微镜(SEM)和JEM-F200型透射电子显微镜(TEM与HRTEM)分析表面形貌;用XSAM800型多功能表面分析系统(XPS)分析元素组成及其价态;用麦克ASAP2460分析仪(BET)测试比表面积;用F-4600型荧光光谱分析仪(PL)检测光生电子与空穴的复合率;用UV-3600型紫外可见分光光度计分析光学吸收性能(DRS)。
将100 mL浓度为10 mg/L 的RhB(目标污染物)倒入烧杯中,加入0.1 g的光催化剂后对混合溶液超声分散10 min再暗态搅拌30 min,然后开启功率为250 W的氙灯作为紫外可见光光源(300~800 nm)照射混合溶液。每隔20 min取样一次,将其离心分离后取上层清液,在λ=553 nm的条件下测试其吸光度A。对RhB的降解率为(A0-At )/A0×100%,其中A0、At 分别为初始和t时刻RhB的吸光度。
2 结果和分析
2.1 XRD谱
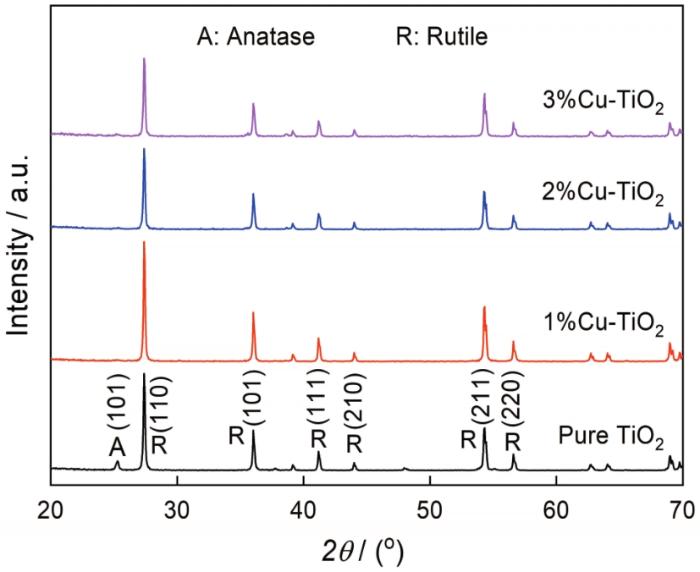
图1给出了纯TiO2和不同浓度Cu-TiO2在650℃热处理后的XRD谱。可以看出,在纯TiO2谱的27.4°、36.0°、41.2°、44.1°、54.3°、56.6°等位置出现了衍射峰,分别对应金红石相的(110)、(101)、(111)、(210)、(211)、(220)晶面。出现在25.3°附近的微弱衍射峰,对应锐钛矿的(101)晶面,表明纯TiO2是由大量金红石以及微量的锐钛矿组成的混晶结构,其中锐钛矿质量分数为6.6%,金红石质量分数为93.4%。在Cu-TiO2的谱中,金红石的衍射峰与纯TiO2类似,但是锐钛矿(101)晶面衍射峰消失,表明Cu掺杂使锐钛矿完全转变为金红石,Cu-TiO2为单一金红石结构。Cu掺杂促进锐钛矿转变为金红石,其原因可能是与Ti离子的半径相近的Cu离子进入晶格取代了Ti离子,晶格常数的改变产生了晶格缺陷,出现的氧空位破坏了晶格的完整性,Ti-O键的断裂促进锐钛矿转变为金红石[15, 16]。纯TiO2、1%Cu-TiO2、2%Cu-TiO2、3%Cu-TiO2金红石的晶粒尺寸分别为49.0、50.8、48.7、45.7 nm。这表明,Cu掺杂对金红石TiO2的晶粒尺寸影响不大。
图1
2.2 纯TiO2 和Cu-TiO2 的形貌
图2给出了纯TiO2(a)及3%Cu-TiO2(b)的SEM照片。可以看出,纯TiO2的颗粒形状各不相同,晶粒尺寸从几十纳米到几百纳米不等。3%Cu-TiO2颗粒尺寸比纯TiO2的大,生成了大块团聚体。
图2
图3
图3
纯TiO2和3%Cu-TiO2的TEM照片
Fig.3
TEM images of pureTiO2 (a, b) and 3%Cu-TiO2 (c, d)
2.3 样品的元素及其化学价态
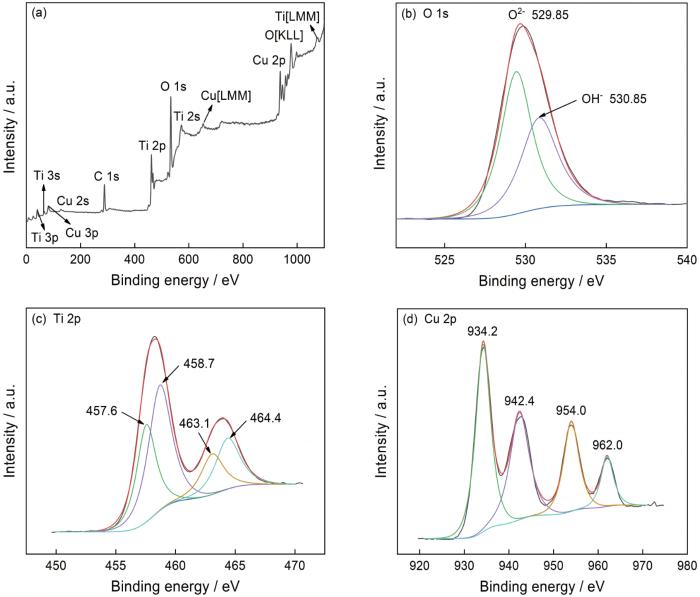
为了分析样品的元素及其化学价态,对3%Cu-TiO2进行了XPS测试,结果在图4中给出。由图4a中的全谱图可见,样品中存在Ti、O、Cu、C元素对应特征峰,C元素主要来源于测试过程中产生的污染。图4b给出了O 1s高分辨谱图谱,谱图中出现了两个O 1s衍射峰。结合能位于529.85 eV处的峰对应于晶格氧(O2-),结合能位于530.85 eV的峰对应于表面羟基氧(OH-)[17]。图4c给出了Ti 2p高分辨谱,由四个峰组成,分别位于457.6 eV、458.7 eV、463.1 eV、464.4 eV,对应于Ti3+ 2p3/2、Ti4+ 2p3/2、Ti3+ 2p1/2、Ti4+ 2p1/2。这表明,Ti元素存在+3、+4价[12, 18]。图4d给出了Cu 2p的高分辨谱,可见Cu2+的特征峰位于934.2 eV和954.0 eV,在942.4 eV和962.0 eV处存在的特征峰对应于Cu+,表明Cu的+1和+2价态共存于样品中[2]。
图4
2.4 纯TiO2 和Cu-TiO2 的N2 吸附-脱附等温曲线和孔径分布
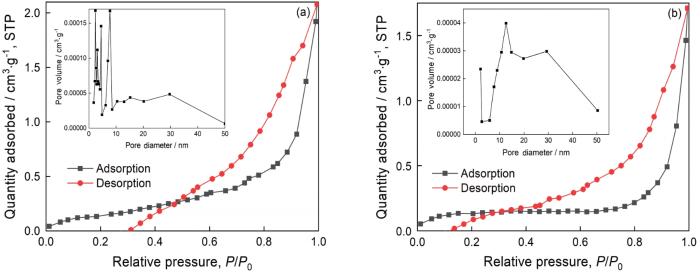
TiO2的形貌对其比表面积有很大影响,决定光催化剂的吸附性能以及活性点位。图5给出了纯TiO2(a)和3%Cu-TiO2(b)的N2吸附-脱附等温曲线及孔径分布图。可以看出,纯TiO2的孔径集中分布5~20 nm之间,比表面积为0.560 m2/g。3%Cu-TiO2的孔径均匀分布在5~30 nm之间,比表面积为0.574 m2/g。这些结果表明,Cu掺杂对TiO2比表面积的影响较小。
图5
图5
纯TiO2和3%Cu-TiO2的N2吸附脱附曲线
Fig.5
Nitrogen adsorption-desorption isotherms of pure TiO2 (a) and 3%Cu-TiO2 (b)
2.5 光催化性能
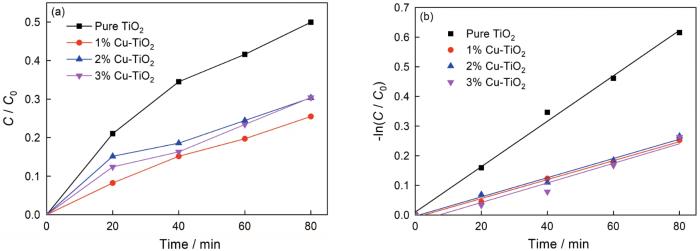
图6给出了纯TiO2和Cu-TiO2对RhB的降解曲线和动力学曲线。可以看出,纯TiO2在80 min后对RhB的降解率为50.0%,Cu掺杂后降解率有所下降,1%Cu-TiO2、2%Cu-TiO2、3%Cu-TiO2的降解率分别为25.5%、30.3%、30.4%。
图6
图6
纯TiO2和Cu-TiO2的降解曲线和动力学曲线
Fig.6
Photocatalytic degradation curves (a) and kinetics curves (b) for pure TiO2 and Cu-TiO2
TiO2光催化剂对RhB的表面降解符合一级反应,其反应速率常数k可根据公式kt=-ln(C/C0 )[5]计算(其中C0和C分别为RhB溶液初始浓度和降解到t时刻的浓度)。反应进行到一定时间后,k值越大表示反应速率越快,样品的光催化性能越好。纯TiO2的一级反应速率常数为0.0077 min-1,1%Cu-TiO2、2%Cu-TiO2、3%Cu-TiO2的降解率分别为0.0032 min-1、0.0032 min-1、0.0033 min-1。这表明,纯TiO2反应速率高于Cu-TiO2,与降解的实验结果一致,Cu掺杂降低了TiO2的光催化反应速率。
2.6 光生电子与空穴的复合
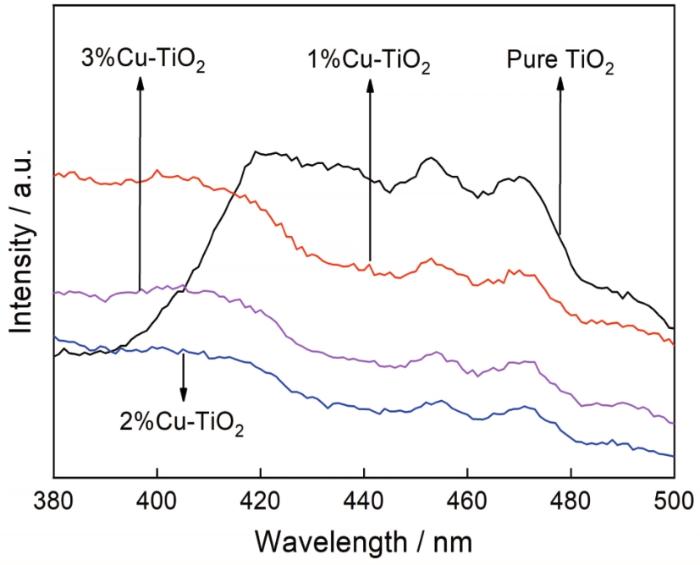
对光催化结果的分析表明,Cu掺杂降低了TiO2的光催化性能。有研究表明,高浓度掺杂会引入过多缺陷,形成的光生电子与空穴新的复合中心反而降低了光生电荷的分离率,从而使光催化剂活性下降[13, 19]。为了分析Cu掺杂对金红石TiO2光生电子与空穴复合的影响,进行了PL光谱测试,结果在图7中给出。由图7可见,Cu掺杂样品的PL光谱强度均下降。其原因是,Cu离子进入晶格内部引入晶格缺陷和形成氧空位。缺陷和氧空位捕获光生电子抑制了光生电子与空穴的复合。随着Cu掺杂浓度的提高PL峰强度先降低后增大,其原因是掺杂高浓度的Cu引入了过多的晶格缺陷和氧空位,反而在TiO2表面形成了光生载流子复合中心,提高了光生电子与空穴的复合率[20~22],2%Cu-TiO2的PL峰强度最低。本文所有浓度的Cu掺杂TiO2的PL峰强度都低于纯TiO2,表明Cu掺杂TiO2的光生电荷分离率高于纯TiO2。因此,Cu掺杂后光催化活性的降低不能归因于Cu掺杂引入了过多的缺陷与空穴,而是形成的新复合中心降低了光生电荷分离率。
图7
2.7 紫外可见吸收光谱
图8
图8
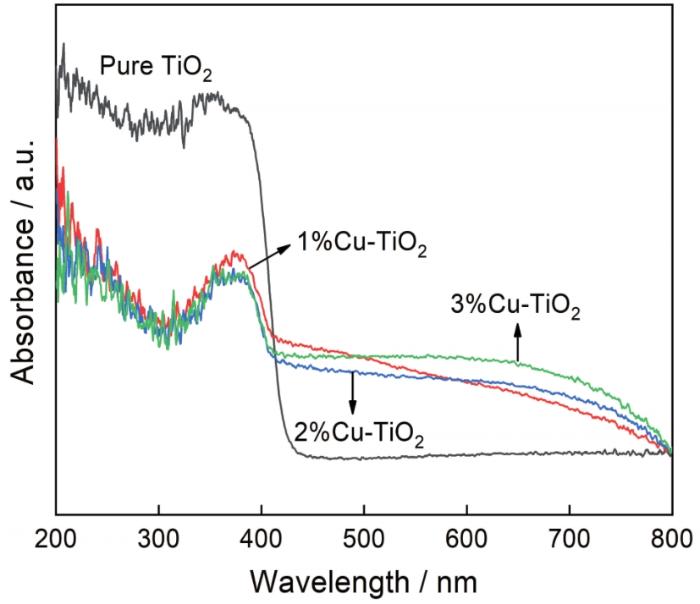
纯TiO2和Cu-TiO2的紫外可见吸收光谱
Fig.8
UV-visible absorption spectra of pure TiO2 and Cu-TiO2
3 结论
Cu掺杂有利于用溶胶-凝胶法制备的Cu-TiO2从锐钛矿向金红石的转变,Cu掺杂TiO2全部为金红石。Cu-TiO2样品中Cu元素以+1和+2价的形式共存。Cu掺杂有利于抑制光生电子与空穴的复合和可见光区域的吸收,但是使光催化活性降低。其原因是, Cu掺杂使TiO2在紫外区域的吸收剧烈下降,从而使其光催化活性降低。
参考文献
Effective photocatalytic degradation and physical adsorption of methylene blue using cellulose/GO/TiO2 hydrogels
[J].
Enhancing photoelectrochemical hydrogen production over Cu and Ni doped titania thin film: Effect of calcination duration
[J].
A comparative study of physicochemical and photocatalytic properties of visible light responsive Fe, Gd and P single and tri-doped TiO2 nanomaterials
[J].
Novel g-C3N4/h'ZnTiO3-a'TiO2 direct Z-scheme heterojunction with significantly enhanced visible-light photocatalytic activity
[J].
Hydrothermal preparation of Ag-TiO2 nanostructures with exposed {001}/{101} facets for enhancing visible light photocatalytic activity
[J].
Preparation and photocatalytic activity of Co-doped TiO2
[J].
钴掺杂改性TiO2的制备及其光催化性能研究
[J].
Treatment of trivalent chromium in electroplating wastewater by Fe (II)-doped TiO2 photocatalyst
[J].
Fe(II)掺杂TiO2光催化剂处理电镀废水中的六价铬
[J].
Photocatalytic degradation and mineralization of microcystin-LR under UV-A, solar and visible light using nanostructured nitrogen doped TiO2
[J].
Photoinduced reactivity of titanium dioxide
[J].
Effects of S and Ta codoping on photocatalytic activity of rutile TiO2
[J]. J.
One-step electrospinning route of SrTiO3-modified Rutile TiO2nanofibers and its photocatalytic properties
[J].
Preparation and characterisation of Ag modified rutile titanium dioxide and its photocatalytic activity under simulated solar light
[J].
Optical, structural and photocatalysis properties of Cu-doped TiO2 thin films
[J].
Photocatalytic degradation of a mixture of eight antibiotics using Cu-modified TiO2 photocatalysts: Kinetics, mineralization, antimicrobial activity elimination and disinfection
[J].
Design of Cu-Ce co-doped TiO2 for improved photocatalysis
[J].
Copper-doped TiO2 photocatalysts: application to drinking water by humic matter degradation
[J].
Influence of heat treatment on photocatalytic activity of Ag-ZnO heterostructure
[J].
热处理对Ag-ZnO异质结构光催化性能的影响
[J].用溶胶-凝胶法制备纯ZnO和Ag修饰ZnO复合光催化剂,并分别对其进行了400℃、450℃、500℃保温2 h的热处理。使用XRD、SEM、TEM、XPS、PL、BET等手段对其进行了表征。结果表明,纯ZnO和Ag修饰ZnO均为六方纤锌矿晶型,Ag颗粒沉积在ZnO表面形成了Ag-ZnO异质结构。以罗丹明B为目标污染物研究了样品的光催化活性。结果表明,热处理温度对纯ZnO的光催化性能的影响较大,在450℃热处理后光催化效果最佳;热处理温度对Ag修饰ZnO的光催化性能没有显著的影响;Ag修饰ZnO比纯ZnO的光催化活性均有所提高,因为Ag修饰提高了ZnO表面羟基的含量并抑制了光生电子与空穴的复合。在500℃热处理后Ag修饰ZnO对罗丹明B的60 min降解率达到98%,其反应速率常数为0.063 min<sup>-1</sup>。
Nitrogen-doped black TiO2 spheres with enhanced visible light photocatalytic performance
[J].
Effect of metal ion doping on the optical properties and the deactivation of photocatalytic activity of ZnO nanopowder for application in sunscreens
[J].
Highly effective Fe-doped TiO2 nanoparticles photocatalysts for visible-light driven photocatalytic degradation of toxic organic compounds
[J].
Enhanced photocatalytic activity of fluorine doped TiO2 by loaded with Ag for degradation of organic pollutants
[J].
Effect of Cu doping on TiO2 nanoparticles and its photocatalytic activity under visible light
[J].