文献标识码: 1005-3093(2017)11-0818-09
通讯作者:
收稿日期: 2016-11-7
网络出版日期: 2017-11-30
版权声明: 2017 《材料研究学报》编辑部 《材料研究学报》编辑部
展开
摘要
使用纳米SiO2作为载体、8-羟基喹啉作为客体制备纳米SiO2/8-羟基喹啉组合物,将其添加到环氧树脂中制备出装载8-羟基喹啉的纳米SiO2/环氧涂层。对其进行盐雾和电化学阻抗谱实验,研究了装载8-羟基喹啉的纳米SiO2/环氧涂层的耐腐蚀机理。结果表明,纳米SiO2/8-羟基喹啉组合物提高了环氧涂层的耐腐蚀性能,添加5%(质量分数)纳米SiO2/8-羟基喹啉组合物的环氧涂层的耐腐蚀性能较优。8-羟基喹啉从纳米SiO2孔道中释放并渗透到涂层与钢基材的界面形成含铁的铬合物膜,阻挡了腐蚀介质的渗入,使Q235钢基体的耐腐蚀性能提高。
关键词:
Abstract
Composites of 8-hydroxyquinoline/nano-SiO2 were prepared with nano-SiO2 as carrier and 8-hydroxyquinoline as modifier. Then the composistes were blended with epoxy resin to form the nanocomposite epoxy coating. The corrosion performance of the prepared composite coating was investigated by means of salt spray test and electrochemical impedance spectroscopy. Results show that composites of 8-hydroxyquinoline/nano-SiO2 can improve the corrosion resistance of the epoxy coatings, among others the coating with 5% (mass fraction) 8-hydroxyquinoline/nano-SiO2 was the optimal. The relevant mechanism may be ascribed to the fact that 8-hydroxyquinoline could release from pores of nano-SiO2 and then penetrate to the interface coating/steel substrate forming Fe-containing complex, thus improving the corrosion resistance of the steel substrate.
Keywords:
涂层能保护金属免受腐蚀,但是在使用过程中发生老化和脱落[1-2]。为了防止涂层的缺陷造成破坏,可在涂层中添加缓蚀剂[3-4]。胡天慧等[5]研究了缓蚀剂酒石酸铈对铝合金(2024-T3)在0.05 mol/L NaCl溶液的作用,酒石酸中的羧基与铝合金基体产生稳定的保护膜,抑制了金属基体的腐蚀。Zong[6]将金属基材浸泡在含有8-羟基喹啉碱性溶液中,在金属基材表面形成致密的防锈层,提高了涂层的耐腐蚀性能。将缓蚀剂直接添加到涂层中,可能导致缓蚀剂与树脂有机官能团反应或不相容,使涂层产生缺陷,影响涂层的防腐蚀性能[7]。纳米粒子使涂层具有优异的耐腐蚀性能和力学性能。将纳米粒子用于涂料的改性,能得到特殊功能,还可大幅度提高涂料抗老化和耐水性。史洪微等[8]将纳米TiO2/SiO2浓缩浆添加到环氧涂层中,以2024-T3铝合金为基体,发现添加1%质量分数的TiO2/SiO2可提高涂层的铅笔硬度和耐腐蚀性能。
本文使用纳米SiO2作为载体,在纳米SiO2孔道中装载缓释剂8-羟基喹啉(HQ),制备纳米SiO2和HQ组合物,然后将其添加到环氧涂层中制备环氧-8-羟基喹啉-纳米SiO2涂层,研究8-羟基喹啉/纳米SiO2组合物对Q235钢材耐腐蚀性能的影响。
在室温条件下,将1 g纳米SiO2(比表面积为150 m2/g,孔径直径为20 nm)溶解100 mL在乙醇溶液中高速分散20 min,以乙醇为溶剂配制0.5 g/mL的HQ溶液100 mL。将配制0.5 g/mL的HQ溶液缓慢的加入到纳米SiO2溶液中,高速分散30 min后抽真空,保持真空5 h后取出产物,用乙醇洗涤5次、离心、干燥,得到淡黄色8-羟基喹啉/纳米SiO2组合物标记为HQ-SiO2。
按配方称取一定量的环氧树脂、稀释剂、助剂,分别加入占组分A质量0%、1%、3%、5%的HQ-SiO2粉体,进行高速分散后球磨6 h,过滤后得到所需涂料组分A。涂料组分B为固化剂聚酰胺,涂料组分A与组分B质量比100∶36。
在Q235钢板(150 mm×75 mm×3 mm)基材表面进行喷砂处理,用空气喷涂方法制备涂层,将其在25℃放置7 d使其固化。涂层干膜的厚度为75±5 μm为膜进行,用于盐雾实验。在Q235钢板(50 mm×50 mm×3 mm)基材表面制备涂层,干膜的厚度为75±5 μm,用于电化学试验。
将添加质量分数为0、1%、3%、5%的HQ-SiO2粉体所制备的装载8-羟基喹啉的纳米SiO2/环氧涂层分别标记为B0、B1、B3、B5。
依据国家标准GB/T 5210-2006,用拉开法测试涂层与基体之间的附着力。在涂层上选取5个点进行测试,测试结果取平均值。依据国家标准GB/T1771-2007,使用浓度为5%NaCl(质量分数)的溶液,试验温度为35±2℃,采用连续喷雾方式进行盐雾实验,盐雾箱的型号为F-750C。使用百分格板评价起泡面积,小泡:肉眼明显可见,直径小于0.5 mm;中泡直径0.6~1 mm;大泡:直径大于1.1 mm。用JEM-2100F透射电子显微镜(TEM) 测试纳米SiO2的粒径,加速电压为200 kV。用ESEMXL30 FEG环境扫描电镜(TEM)观察涂层的微观形貌。用ESEM所携带的附件 EDX 分析腐蚀产物中元素的种类和含量。根据电化学阻抗谱(EIS)对涂层进行电化学测试分析。使用KBr压片法制备样品进行红外光谱分析(IR),扫描范围400~4000 cm-1,红外光谱分析仪的型号BRUKER IFS55。使用273A电化学阻抗测试系统测试电化学阻抗谱(EIS),测量频率范围为100~10 MHz,测量信号为幅值10 mV的正弦波。使用三电极体系电解池,辅助电极为铂电极,参比电极为饱和甘汞电极(SCE),涂层/基体试样为工作电极,工作电极的有效面积约为12.56 cm2,腐蚀介质为3.5%NaCl溶液。用ZSimpWin阻抗分析软件进行处理交流阻抗数据。使用UV2100紫外分光光度计,扫描范围为190~400 nm,HQ在202 nm波长处有最大吸收峰,选择在202 nm波长处测定HQ-SiO2溶液中HQ的浓度。将0.1 gHQ-SiO2溶于250 mL无水乙醇(溶剂)中,在室温匀速搅拌后每间隔30 min取样5 mL。测定释放液中HQ的吸光度,计算HQ释放量,测试不同时间段溶液中HQ特征吸收峰强度,每个时间段测试3次,通过吸光度与浓度的线性方程计算HQ-SiO2中的HQ释放浓度。使用SVPIOO测试系统,探针振幅(Vibration Amplitude)为3 μm,有机涂层的腐蚀失效是从涂层缺陷开始,用尖针在涂层表面制造人为缺陷的试样,缺陷直径约为1 mm,露出基体。
图1给出了纳米SHQ-SiO2TEM测试结果。从图1a可以看出,纳米SiO2孔的尺寸比较均一。图1b显示,HQ-SiO2尺寸约为20~30 nm。
图1 纳米SiO2和HQ-SiO2的TEM像
Fig.1 TEM image of nano-SiO2 and HQ-SiO2 particles (a) nano-SiO2; (b) HQ-SiO2
称取HQ,配制30 mg•L-1HQ的乙醇标准溶液。量取标准液并分别稀释至 20、40、50、60、80、100倍,以乙醇作空白对照,用紫外光度计在202 nm测定其吸光度,绘制标准曲线,其线性回归方程A=0.193C+0.0734,r=0.0992为相关系数,A为紫外吸收值,C为HQ浓度。用差减法计算HQ在纳米SiO2中的负载量为275.7 mg•g-1。
根据吸光度与浓度拟合线性曲线公式[9]计算8-羟基喹啉的释放百分率

其中 
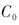

图2给出了HQ-SiO2在标准溶液中的释放曲线,使用标准曲线线性拟合方程计算。在浸泡初期,HQ-SiO2中缓蚀剂 HQ 从SiO2孔道中释放到乙醇溶液中并出现明显的初始突释现象。这表明,溶液中HQ的浓度差致使HQ-SiO2组装体中装载在SiO2孔道外壁或者表面的HQ首先释放,产生突释现象。随着浸泡时间的延长HQ缓慢从SiO2孔道中释放出来,使溶液中HQ的浓度增大,浸泡100-120 h时HQ-SiO2溶液中的HQ浓度释放率比较平稳,说明大部分HQ已从HQ-SiO2组合物中释放出来。
图2 不同时间纳米SiO2载体负载8-羟基喹啉释放曲线
Fig.2 Different time of release curve the 8 - hydroxyquinoline from nano-SiO2
提高基体与涂层的附着力是涂层性能的重要参数。在胶黏剂和拉伸速度相同的前提下用拉开法测试的B0、B1、B3、B5 涂层的附着力,结果列于表1。
表1 B0、B1、B3、B5四种涂层的拉开法附着力测试结果
Table 1 Pull-off test results of adhesion of the B0、B1、B3 and B5 coatings (MPa)
| Sample | 1 | 2 | 3 | 4 | 5 | Mean |
|---|---|---|---|---|---|---|
| B0 | 6.8 | 6.7 | 6.8 | 6.5 | 6.1 | 6.58 |
| B1 | 7.2 | 7.2 | 7.3 | 7.6 | 6.9 | 7.24 |
| B3 | 7.5 | 7.8 | 7.5 | 7.9 | 8.2 | 7.78 |
| B5 | 7.6 | 7.8 | 8.3 | 8.5 | 8.7 | 8.18 |
从表1可见,B0涂层的附着力为6.58 MPa,B1涂层的附着力为7.24 MPa,B3涂层的附着力为7.78 MPa,B5涂层的附着力为8.18 MPa。随着涂层中HQ-SiO2含量的提高装载8-羟基喹啉的纳米SiO2/环氧涂层与基材之间附着力随着提高。
由于HQ-SiO2中的羟基在金属基体表面形成H键,脱H2O反应后形成-Si-O-M(金属)共价键,HQ中的-OH在水解条件下与SiO2形成Si-OH,Si-OH分子间又可相互缩合为Si-O-Si 链,聚合形成网状结构的膜,提高了其与环氧树脂涂层的结合力,进一步提高了环氧树脂涂层的耐腐蚀性能,具有抗外界酸、碱、盐等腐蚀的特性。
图3给出了添加不同含量HQ-SiO2环氧涂层试样盐雾实验1000 h后的照片,图4给出了装载8-羟基喹啉的纳米SiO2/环氧涂层试样盐雾实验1000 h后划痕处横截面部位SEM图。
图3 涂层试样盐雾实验1000 h后的照片
Fig.3 Photos of the coated panels after salt spray tests for 1000 h (a) B0, (b) B1, (c) B3 and (d) B5
表2给出了涂层盐雾实验1000 h后装载8-羟基喹啉的纳米SiO2/环氧涂层腐蚀状态。盐雾实验1000 h后各涂层表面划痕处均出现不同程度的腐蚀和起泡现象,B0涂层腐蚀最严重,腐蚀产生的小泡面积为85%,中泡面积为5%,划痕处腐蚀扩展平均宽度7.6 mm,B1涂层小泡面积为15%,中泡面积为1%,划痕处腐蚀扩展平均宽度为7.3 mm,B3涂层小泡面积为5%,中泡面积为1%,划痕处腐蚀扩展平均宽度为5.6 mm,B5涂层腐蚀程度最小,没有小泡产生,中泡面积为1%,划痕处腐蚀扩展宽度最大为6.5 mm。从图3可以看出,添加纳米HQ-SiO2涂层耐腐蚀性能得到改善,在本实验中B5涂层的耐盐雾腐蚀性能最佳。
表2 盐雾实验1000 h后涂层试样的腐蚀情况
Table 2 Corrosion situation of coated panels after salt spray tests for 2000 h
| Sample | Small bubble area% | Mid-bubble area/% | Big bubble area/% | Average width of corrosion expansion/mm |
|---|---|---|---|---|
| (a) | 85 | 5 | 0 | 7.6 |
| (b) | 15 | 1 | 0 | 7.3 |
| (c) | 10 | 1 | 0 | 5.6 |
| (d) | 0 | 1 | 0 | 6.4 |
图4给出了盐雾实验1000 h后试样划痕截面SEM图。盐雾1000 h后四种涂层试样划痕处均出现不同程度的腐蚀现象,B0涂层划痕处基体腐蚀程度最为严重,划痕处基体腐蚀深度为289 μm,B1涂层划痕处基体腐蚀深度为190 μm,B3涂层基体划痕处腐蚀深度为93 μm,B5涂层试样基体腐蚀深度为24 μm,B5环氧涂层同样表现较好的耐腐蚀性能。
图4 涂层试样盐雾实验1000 h后划痕处横截面SEM图
Fig.4 SEM images of the scribe sections of (a) B0, (b) B1, (c) B3 and (d) B5 coated samples after 1000 h salt spray tests
2.5.1 EIS谱图分析图5给出了装载8-羟基喹啉的纳米SiO2/环氧涂层试样添加不同含量HQ-SiO2粉体在3.5%NaCI溶液中浸泡不同时间的EIS图谱。
图5 不同含量HQ-SiO2环氧涂层试样在3.5%NaCl溶液中浸泡不同时间的Bode图
Fig.5 Bode plots of coated panels with different loading of HQ-SiO2 after different immersing times in 3.5%NaCl solution (a) B0, (b) B1, (c) B3 and (d) B5
图5a给出了B0涂层试样在3.5%NaCI溶液中浸泡不同时间EIS图谱。可以看出,在3.5%NaCI溶液中浸泡180 h后B0涂层试样的阻抗降低,随着浸泡时间的延长涂层阻抗值降低,当浸泡时间为720 h后阻抗出现最低值107Ω•cm2。B1涂层在3.5%NaCl溶液中阻抗值浸泡350 h时涂层阻抗值降低,浸泡500 h出现上升趋势,随着浸泡时间的延长阻抗值降低。B3涂层试样在浸泡过程中出现缓慢下降,随着浸泡时间的延长涂层阻抗值保持在107Ω•cm2以上。在整个浸泡过程中B3阻抗值高于B0、B1涂层,B5涂层阻抗值高于B3、B1、B0涂层。随着环氧涂层中纳米HQ-SiO2粒子含量的提高涂层的耐腐蚀性能越好。其原因是,环氧涂层中纳米HQ-SiO2粒子阻碍NaCl溶液腐蚀介质的渗透,环氧涂层中的缓蚀剂HQ从SiO2孔道中释放到基体表面,HQ与金属碳钢基体表面产生物理吸附、化学吸附和对腐蚀介质的抑制作用[9],因此,随着装载8-羟基喹啉的纳米SiO2/环氧涂层中HQ-SiO2含量的提高环氧涂层的耐腐蚀性能提高。
为了更深入的分析腐蚀机理,根据图5所示的等效电路图对4种涂层阻抗谱图进行拟合,其中高频段时间常数代表了涂层的特性,低频段时间常数代表涂层下金属界面腐蚀的特性。对不同浸泡时间的4种涂层的腐蚀阻抗谱图进行拟合,B1、B3和B5涂层在整个浸泡过程的等效电路图为R(QR),B0涂层在浸泡过程中等效电路图为R(QR),浸泡后期为R(Q(R(QR))),其中Rs为溶液电阻,Qc为涂层表面腐蚀介质界面常相位角元件,其中参数n=0时代表纯电阻,n=1时代表纯电容,Rc为涂层孔隙电阻,Rt为转移电荷电阻,反映涂层与基材界面间的信息,Qv为金属基材与腐蚀介质间的界面电容。图6给出了添加HQ-SiO2粉体环氧涂层电阻随浸泡时间的变化曲线。可以看出,在浸泡初期B5涂层电阻最高,B1涂层电阻最低,浸泡180 h后电阻值出现迅速下降波动趋势,浸泡到350 h后B5涂层电阻值大于B0、B1、B3涂层电阻,B0涂层电阻最小,B5的电阻值最高。
图6 等效电路图
Fig.6 EEC models for the coated panels at different immersion stages,(a) equivalent circuit for the intact coating has one time constant and(b)equivalent circuit for the coating have two-time constant
2.5.2 SVET研究装载8-羟基喹啉的纳米SiO2/环氧涂层缺陷处腐蚀电化学行为通过对盐雾实验结果和EIS阻抗的分析,B5涂层耐腐蚀性能最佳。因此对B5涂层进行SVET测试,研究涂层缺陷处局部腐蚀电化学行为。图8给出了有人造缺陷的B5涂层SVET面扫实验结果。
图8给出了人造缺陷的添加HQ-SiO2环氧涂层钢体系在浓度为3.5%NaCl溶液中浸泡不同时间SVET原位监测结果和装载8-羟基喹啉的纳米SiO2/环氧涂层浸泡不同时间基体腐蚀电流密度分布图。可以看出,缺陷处表现出较强的电化学活性,并且随着浸泡时间的延长涂层电流密度随着变化。浸泡1 h时缺陷处最大腐蚀电流密度为12 μA/cm2,浸泡2 h时缺陷处最大腐蚀电流密度增加20 μA/cm2,浸泡3 h时缺陷处最大腐蚀电流密度为8 μA/cm2。电流密度出现的下降的原因是,HQ-SiO2在浸泡初期HQ产生突释现象,使HQ对人为制造的缺陷处产出缓释作用。浸泡时间为36 h时涂层缺陷处腐蚀电流密度增到140 μA/cm2,达到最大值。这个结果表明,缺陷处暴露的金属基体逐渐溶解,腐蚀越来越严重。浸泡43 h时缺陷处腐蚀电流密度由140 μA/cm2下降到110 μA/cm2,因为随着浸泡时间的进一步延长,缓释剂HQ从纳米SiO2孔道中大量释放到涂层中,在金属表面发生吸附作用,覆盖在金属表面或者金属表面的活性部位,改变了金属在介质中的双电层结构,提高了金属离子化的活化能,从而抑制金属的电化学腐蚀[10]。在腐蚀过程中产生的腐蚀产物阻碍腐蚀介质的渗入,使电流密度变小。
图8 Q235钢表面带有人造缺陷的5% HQ-SiO2环氧涂层在3.5%NaCl溶液中电流密度分布图
Fig.8 Current mapping of the 5% HQ-SiO2 epoxy coated steel with an artificial defect immersed in 3.5%NaCl solution Current density distribution
图9给出了B5涂层盐雾实验1000 h后涂层与腐蚀基体界面生成物红外光谱。从红外光谱图9a可以看出,吸收谱峰值3040 cm-1为HQ的C-H伸缩振动,1572 cm-1、1498 cm-1、1463 cm-1(芳环C= C骨架伸缩振动),3022 cm-1附近的吸收为H2O的O-H伸缩振动峰,1600 cm-1和1570 cm-1的吸收峰归属于喹啉环的C=C特征振动峰,600~800 cm-1范围内的峰为喹啉环的特征振动吸收峰。
图9 红外光谱图(a)8-羟基喹啉(b)二氧化硅装载8-羟基喹啉(c)腐蚀产物
Fig.9 IR diagrams, (a) HQ,(b) HQ- SiO2, (c) corrosion products
图9b给出了HQ-SiO2红外吸收光谱图。8-羟基喹啉装载到SiO2孔道中,红外吸收光谱峰值中8-羟基喹啉的特征峰值减弱。图9c给出了涂层盐雾实验后涂层与基体界面的红吸收光谱图。可以看出,红外吸收光谱的特征振动模式为3421 cm-1处的宽峰为OH-的伸缩振动特征峰,3065 cm-1处的峰值对应芳香环内C-H键的伸缩振动,1709 cm-1、1627 cm-1处尖峰对应芳香环内-C=C-键的骨架伸缩振动,1588 cm-1、1509 cm-1、1473 cm-1、1435 cm-1、1405 cm-1处的峰对应芳香环骨架的特征吸收峰,1381 cm-1、1292 cm-1处的峰对应-C-N-键的伸缩振动,278 cm-1、1164 cm-1处的峰对应-C-O键的伸缩振动,600~800 cm-1范围内的峰对应喹啉环的特征振动吸收峰;400~600 cm-1范围内的峰处于远红外区,对应金属Fe3+与HQ配位体之间的振动吸收。1588 cm-1附近的特征峰说明该分子中芳香环的共轭作用很强,即整个喹啉环上的电子轨道杂化呈P键。-C-O键对应振动吸收峰1278 cm-1、1164 cm-1比HQ红外吸收谱中的相应的峰变窄、变弱。这些结果表明,HQ与Fe3+发生了配位,400~700 cm-1处峰强度弱。其原因是,HQ从SiO2孔道中释放出来,渗透到基体表面直接与基体Fe的氧化物Fe3+作用生成络合物(C9H8ON)3Fe,产生的络合物吸附在基体表面形成了络合物,阻止了腐蚀介质对基体的再次腐蚀,从而提高了涂层的耐腐蚀性能能[11]。
其产生络合物反应方程式为
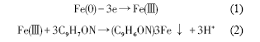
8-羟基喹啉对碳钢有良好的缓蚀效果。使用纳米SiO2装载缓蚀剂8-羟基喹啉制备的组合物,将其添加到环氧涂层中可制备装载8-羟基喹啉的纳米SiO2/环氧涂层。添加不同质量分数HQ-SiO2制备的B0、B1、B3和B5涂层,其耐腐蚀性能的排序为B5>B3>B1>B0。B5涂层的耐腐蚀性能最佳,B0涂层耐腐蚀性能最差。装载8-羟基喹啉的纳米SiO2/环氧涂层中纳米SiO2装载的HQ与基体腐蚀产物Fe3+发生反应,形成8-羟基喹啉与铁的络合物吸附在基体表面,阻挡腐蚀介质的与基体的接触,从而提高了涂层对钢基体的耐腐蚀性能。
The authors have declared that no competing interests exist.

/
| 〈 |
|
〉 |